Temps estimé de lecture: 25mn
Aujourd’hui, les scientifiques sont débordés par le problème de la preuve dans le contexte du procès “santé contre industriels”, car la causalité disruptive des perturbateurs endocriniens rend inopérants les critères habituels de mesure de la relation de cause à effet. Les mécanismes d’action des perturbateurs endocriniens, dont l’intensité d’exposition n’est pas proportionnelle à l’intensité de l’effet, démentent le gradient biologique de la relation dose effet ainsi que la stabilité de l’association, sur quoi reposent les critères de la toxicologie unanimement reconnus. La réalité physiopathologique déborde les modèles imparfaits élaborés pour des problèmes plus simples, et cette difficulté de nature scientifique sert si bien les intérêts de la défense industrielle, qu’elle appuie de tout son poids sur ce levier, contre la sécurité des personnes.
Les perturbateurs endocriniens ont tardé à être révélés (en 1991, déclaration de Wingspread[1], car ils bouleversent le modèle de causalité traditionnel. Leur effet consiste à troubler les systèmes de communication qui au sein de l’organisme, organisent son équilibre, son maintien en vie et en bonne santé. Ou bien ils modifient la quantité d’hormones sécrétées, ou bien ils modifient la réponse des cellules cibles de ces hormones, signaux chimiques, qui régulent et coordonnent l’ensemble des fonctions physiologiques de l’organisme, avec des conséquences multiples.
Mais surtout, leur effet peut être indépendant de la dose absorbée : au pire, la plus petite unité de présence détectable de la substance incriminée peut générer un effet délétère majeur, qui dépend des processus en cours au sein de l’organisme. Ainsi la même dose qui sera sans effet sur un adulte pourra provoquer une maformation génitale grave sur un embryon, ou programmer un cancer chez le foetus, qui se déclarera 30 ans plus tard, et dont il transmettra le risque à sa descendance. Les notions de fenêtre critique, et de seuil absolu se sont imposées pour rendre compte d’effets observés chez les animaux et les végétaux d’abord. Ce n’est qu’”à posteriori”, à partir de l’observation de phénomènes dont l’épidémiologie classique ne pouvait rendre compte, que les hypothèses sur les mécanismes d’action des perturbateurs endocriniens ont été formulées. “Dès lors, ce n’est sans doute pas de l’épidémiologie qu’il faut attendre une preuve irréfutable entre certaines maladies et l’exposition à des perturbateurs endocriniens mais de leur conjonction avec d’autres données recueillies in vivo et in vitro”[2]. Ce bouleversement épistémologique explique le retard à la réglementation, puisque depuis 2009 la Commission Européenne, manipulée par les lobbies industriels, enlise la politique de protection des populations vis à vis des perturbateurs endocriniens avec la question des critères de définition de ces substances.
Mécanismes d’action des perturbateurs endocriniens
Mécanisme toxique
Un perturbateur endocrinien n’a pas un effet nocif déterminé par ses propriétés physico-chimiques ou cinétiques[3]. Il n’y a pas une relation univalente entre la cible dans l’organisme et le perturbateur. Son effet est déterminé par la fonction de la cellule sur laquelle il s’applique comme un leurre. Transposé dans l’univers informatique, le perturbateur endocrinien serait un hackeur capable de s’introduire sur des sites protégés. L’action qu’il déclenchera dépendra de la nature du site : sur le site d’une banque, il pourra détourner ou créer de l’argent à son profit ; sur un site militaire, il pourra déclencher une attaque armée.
Ainsi, le perturbateur endocrinien, d’une part, en se fixant sur un récepteur hormonal d’une cellule cible, agit comme un leurre et déclenche une réponse qui est elle-même variable. Il peut soit déclencher une action hormone-like (agoniste), soit bloquer le récepteur (action antagoniste); il peut agir sur le mécanisme de régulation de la production hormonale par les cellules sécrétrices, et modifier la concentration d’hormones, qui détermine l’intensité de la réponse hormonale (2 p.13).« Les perturbateurs endocriniens mettent en jeu les mécanismes de signalisation, de régulation et d’action physiologiques plutôt que les mécanismes classiques de la toxicité conduisant au dysfonctionnement ou à la mort cellulaire »[4].
Les cibles d’un perturbateur endocrinien sont multiples

“A l’heure actuelle les travaux utilisant des technologies de génomique dégagent essentiellement des « signatures » de perturbateurs sans apporter encore un lien de causalité entre la variation d’expression des gènes identifiés et la survenue de pathologies. Plusieurs études ont montré que des perturbateurs endocriniens peuvent induire des signatures différentes de celles des ligands endogènes, notamment les œstrogènes. Cela renforce la notion que ces perturbateurs ont une vaste gamme d’effets qu’il faut étudier en tenant compte de leur spécificité d’action et de la multiplicité des cibles possibles. L’idée d’un lien simple entre perturbation endocrinienne, action œstrogénique et reprotoxicité doit être abandonnée, la situation apparaissant bien plus complexe”, selon le rapport de l’INSERM en 2011 (4 p.151).
La relation dose effet n’est pas linéaire : la toxicité n’a pas de valeur seuil inférieure
La quantité d’hormones nécessaire au fonctionnement du système endocrinien est extrêmement faible, de sorte qu’une très faible concentration de susbtances perturbatrices suffit pour perturber son fonctionnement[5] “ L’un des premiers points de contestation de l’application des principes traditionnels aux perturbateurs endocriniens est l’affirmation selon laquelle ils seraient susceptibles d’agir à de très faibles doses voire même d’agir par simple présence. On serait alors dans la logique du tout ou rien, le perturbateur agissant comme une clef dans une serrure : sa seule présence suffirait pour l’actionner et déclencher la perturbation” (2 p.74). L’exposition à de très petites doses est déjà toxique : la règle habituelle de la relation proportionnelle entre la dose et l’effet n’est plus pertinente pour les perturbateurs endocriniens : on observe des effets pour des doses très faibles. Plus précisément on parle d’une relation dose effet non monotone, qui révèle une toxicité marquée à une dose extrêmement faible voire à une simple exposition à la substance 2 et (4 p.141).“Le mot « la dose », suggérant une gradation allant de la dose minime à la dose massive, risque de masquer que des microdoses peuvent être dangereuses, de laisser entendre à tort qu’une dilution peut suffire pour venir à bout de l’effet d’un poison – ce qui est inexact, d’autant plus que certains n’ont même pas d’antidotes – et de masquer que des effets mortels peuvent résulter de doses minimes d’un produit qui ne ressemble pas à un poison”[6].
En matière de faibles doses plusieurs études ont montré la toxicité du Bisphénol A pour des doses inférieures aux doses journalières admissibles (DJA). Des rongeurs à des doses très faibles de Bisphénol A, très inférieures à la DJA, développent des lésions précancéreuses du sein, des cancers in situ à des doses plus élevées… D’autres études ont fait le constat que les rates exposées à 50 µg/kg de BPA pendant les quatre premiers jours de vie ont un cycle ovulatoire qui s’interrompt prématurément et leur cycle devient irrégulier dès l’âge de deux mois et demi. D’autres résultats sur l’âge du déclenchement de la puberté mettent en évidence les potentiels effets paradoxaux : avancement de l’âge à faible dose, recul à forte dose. “Cette observation n’est pas isolée pour les perturbateurs endocriniens puisqu’il peut être observé un effet à faible dose et une absence d’effet à forte exposition, la courbe dose réponse n’est pas alors en croissance linéaire ou exponentielle mais forme une courbe inversée. L’effet est paradoxal” (2 p.76). Selon Barbara Domeinex, l’effet dose faible supérieur à la dose forte peut être lié à deux mécanismes : une dose très faible passe sous le radar de la fonction hépatique, qui ne détoxique pas, et laisse agir la molécule, alors que pour une dose supérieure, le foie la détruirait ; c’est une réaction au niveau de l’organisme entier. Le second mécanisme est cellulaire : pour une dose faible la cellule ne réagit pas, alors qu’elle produit une réaction élevée sur une dose forte[7].
Le critère de Dose Journalière Admissible n’est donc plus pertinent : la simple présence peut être toxique, l’exposition chronique peut aboutir à une accumulation toxique pour l’organisme ; les effets paradoxaux d’une toxicité plus élevée à faible dose qu’à forte dose empêchent de soutenir l’existence d’une exposition sans effet. L’éviction totale de certaines substances est la seule réponse efficace. Les conséquences en matière de processus réglementaire sont radicales, et les résistances du monde industriel massives.
L’effet varie selon l’état de l’organisme exposé
Les effets des perturbateurs endocriniens sont variables, en fonction du sexe, de l’âge, de la durée d’exposition ; ils prennent en défaut les méthodes d’évaluation de la toxicologie classique 2 (6 p.4) ([8] p.12). On parle d’effet Fenêtre, pour évoquer les périodes critiques d’exposition, qui concernent le développement pré-natal et la puberté.
Les maladies d’induction foetale
La période de développement des organes et de la mise en place des marques épigénétiques dans les gamètes est une période de grande vulnérabilité. La dangerosité de l’exposition n’est pas identique pour un foetus, un bébé, un enfant, un adolescent ou un adulte. Les conséquences seront de nature et de gravité différentes. Ainsi un foetus masculin contaminé in utero pendant le premier trimestre de la grossesse risque des malformations de l’appareil urogénital : cryptorchidie, monorchidie, hypospadia. Il présente des risques majorés de cancers du testicule et de la prostate qui s’exprimeront des années plus tard, à l’âge adulte (2 p.81) “Certaines étapes essentielles de l’embryogenèse ne durent que quelques jours, voire une journée, ce qui signifie que peut être retenue la journée comme période critique à l’exposition, éventuellement unique, à un produit toxique” ([9] p.31). “Cela a des implications importantes en ce qui concerne l’exposition domestique à des polluants qui est par nature le plus souvent de courte durée. Cela plaide pour une évaluation globale de l’exposition des personnes au lieu de la seule surveillance de la pollution des milieux” (9 p.31).
L’action des perturbateurs pendant les stades de différenciation tissulaire va avoir des conséquences à long terme sur la reproduction de l’individu adulte et sa descendance en perturbant l’organogenèse des tissus et en induisant des modifications épigénétiques dans les gamètes durant cette période[10]. Les expositions in utero peuvent avoir des effets à long terme, non seulement au cours de la vie de l’individu, mais sur sa descendance : démonstration en a été faite jusqu’à la 3e génération pour un mélange de plastifiants chez les rongeurs et pour le diéthylstilbestrol (DES) dans l’espèce humaine[11]. Dès l’enfance, des troubles du comportementaux peuvent apparaître chez les petits garçons de 3 à 5 ans, en proportion avec le niveau d’exposition de leur mère à certains perturbateurs endocriniens, comme l’a montré une étude de l’INSERM publiée en 2017[12].
Délai très retardé entre l’exposition et certains effets
Les risques de cancers de l’appareil génital et hormono-dépendants (testicules, prostate, sein, ovaire) sont augmentés par les perturbateurs endocriniens, mais leur action, qui peut se dérouler pendant la formation du foetus, ou plus tardivement dans le développement de l’enfant, n’exprimera ses conséquences que plusieurs décennies plus tard, sous forme de tumeurs cancéreuses 10 (5 p.12).
Effet cocktail des mélanges complexes
La multiplicité des sources de perturbateurs endocriniens (médicaments, produits ménagers, meubles, aliments, produits d’hygiène…), les multiples voies d’exposition (orale, cutanée, respiratoire), le cumul des doses et l’interaction des substances soumettent l’organisme à une situation dont la toxicologie classique ne peut rendre compte. “ Il n’y a pas dans l’environnement de dose pure. Nos concitoyens ne sont pas exposés à un seul produit mais à une multitude, à des doses plus ou moins fortes, de manière chronique. Le seul moment où l’on retrouve des conditions de laboratoire et où un homme ou une population sont exposés à une dose toxique d’un seul produit prépondérant sont les accidents industriels type Seveso” 2 p.77. C’est la dose totale reçue qui doit être considérée pour évaluer ses impacts sur la santé. Or, “les méthodes d’évaluation du risque cumulatif pour la santé, lié à des expositions combinées butent sur le caractère limité des connaissances scientifiques actuelles. D’où le silence des guides méthodologiques nationaux sur les méthodes d’évaluation du risque cumulatif pour la santé, lié à des expositions combinées” (9 p.32).
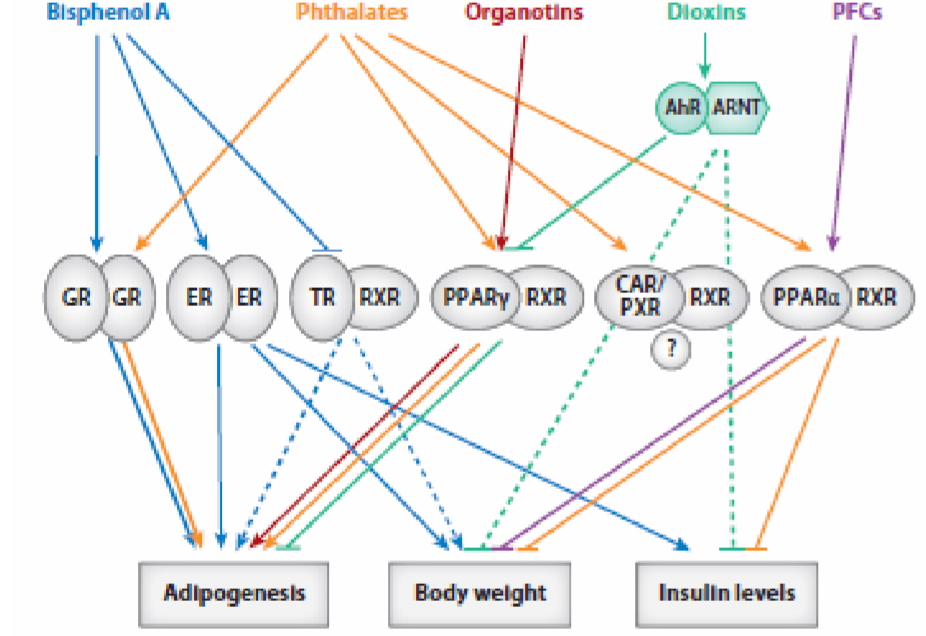
“Cette réalité de la multi-exposition est d’autant plus difficile à appréhender que le système endocrinien est très complexe. Une molécule peut avoir plusieurs effets différents agonistes ou antagonistes avec plusieurs récepteurs, le problème se démultipliant avec le nombre de polluants examinés. Ce schéma permet de saisir visuellement l’extrême complexité des mécanismes potentiellement à l’œuvre” (2 p.77).La méthode toxicologique classique qui évalue la toxicité de chaque molécule individuellement ne peut rendre compte de cette réalité complexe. Les scientifiques envisagent aujourd’hui 3 types de modèles d’interaction dans les mélanges complexes de perturbateurs endocriniens (2 p.79) :
L’addition des concentrations: Modèle 0+0+0=3
Des « perturbateurs endocriniens de la même catégorie » ont des effets globalement additifs ou cumulatifs. Ainsi, à une dose donnée, isolés, plusieurs composés peuvent ne pas avoir d’effet mais, réunis, ceux-ci peuvent perturber le développement d’un tissu (4 p.157). “Dans ce cas, l’effet du mélange est l’effet d’un des composés à la concentration correspondant à la somme des concentrations des produits présents dans le mélange. De sorte que, un tel mélange peut avoir un effet alors que tous ses composés se trouvent à une concentration inférieure à la dose sans effet observé” (2 p.79). “ Une des illustrations les plus probantes qui alimente ce débat est l’effet de substances considérées comme « antiandrogéniques ». Il a été montré que la flutamide, la vinclozoline ou la prycymidone peuvent à doses faibles ne pas modifier la distance anogénitale, un critère de la masculinisation mâle mais que le mélange de ces substances diminue significativement ce paramètre… De même, chez le fœtus de rat, trois phtalates différents qui individuellement n’induisent aucune hypospadia peuvent en combinaison induire des hypospadias chez la moitié des ratons” (4 p.157).
Une étude française (9) a montré un effet additif (et non synergique) des anti-androgènes sur le développement testiculaire de cellules embryonnaires humaines. Cet effet additif (1+1=2) n’a pas la puissance de l’effet cocktail (1+1=3), mais révèle par l’effet cumulé des substances chimiques auxquels les organismes sont aujourd’hui confrontés, l’insuffisance du modèle toxicologique classique qui mesure l’impact de chaque molécule isolément[13].
L’addition des réponses: Modèle 1+1=2
Le second modèle concerne les mélanges plus complexes impliquant des perturbateurs endocriniens considérés comme de catégories différentes (avec des mécanismes d’actions différents). Dans ce cas, les effets semblent beaucoup moins prévisibles et sont moins bien compris (4 p.157). “Dans ce modèle toxicologique, l’effet du mélange est la somme des effets de chaque composé à la dose considérée. Ainsi, un mélange de composés en dessous de la dose sans effet observé est lui-même sans effet. L’approche toxicologique classique suppose que ce modèle s’applique lorsque les substances ont des voies d’action différentes” (2 p.79). “ Un exemple de ce genre est la récente étude d’Eustache et coll. (2009) qui ont administré un mélange de génistéine, un phyto-œstrogène, et de vinclozoline à des doses « faibles » ou « fortes » à des rats depuis la vie fœtale jusqu’à l’âge adulte. Dans ces conditions, le mélange à doses faibles peut diminuer plus fortement le nombre de spermatozoïdes que le mélange à doses fortes. Par ailleurs, à doses faibles, le gavage avec un seul de ces composés n’altère pas ce paramètre. Notons enfin, que ce type d’exposition artificielle est encore loin de reproduire la complexité de la multitude de substances potentiellement reprotoxiques auxquelles l’être humain peut être exposé. Très peu d’études ont tenté d’aborder la question de l’exposition à un mélange complexe de polluants environnementaux reflétant une situation réelle. Citons dans ce cadre le travail de Fowler et coll. (2008) qui démontre que l’élevage de brebis gestantes sur des pâturages « fertilisés » avec des boues d’épandage altère le développement ovarien. Il semble donc qu’un mélange reflétant une exposition complexe humaine (boues provenant des égouts) puisse altérer la fertilité. Évidemment la détermination de(s) substance(s) active(s) et impliquée(s) est dans ce cas plus compliquée” (4 p.157).
La potentialisation des produits les uns par les autres : Modèle 1+1=3
“Plusieurs études récentes conduites en laboratoires in vivo ou in vitro…montrent que l’administration de plusieurs produits à des rongeurs à des doses sans effets, prises individuellement, provoque un effet très marqué, administrées conjointement. L’étude d’Ulla Hans montrait ainsi que la combinaison de trois produits en dessous de leur limite sans effet pouvait conduire chez des rates gestantes à une progéniture qui, pour les mâles, souffrent à 60 % de malformations génitales du type de l’hypospadias. L’existence d’un effet de potentialisation des différents produits entre eux pose de très importantes difficultés” (2 p.79). La synergie des effets (1+1=3) correspond non pas à une simple addition des effets, qui concerne des perturbateurs de même famille, ni à la juxtaposition des effets de chaque substance, mais à un effet spécifique de facilitation de l’action d’une molécule par une autre, que la complexité des mélanges dans l’environnement rend particulièrement difficile à identifier.
Les combinaisons toxiques
Ensuite se pose la question de la détermination des combinaisons toxiques. “Quelles sont-elles ? La toxicité provient-elle de la seule combinaison de produits chimiques ou est-elle déclenchée par d’autres facteurs extérieurs physiques (champ magnétique…) ou propres à l’individu (prédisposition génétique, stress…)” (2 p.80).
Concernant la fertilité masculine, les agents physiques comme la chaleur, les rayonnements ionisants ou la lumière impactent la production de testostérone. Les testicules doivent être à une température inférieure de 2 à 3°C de celle du corps. Une élévation de la température corporelle liée à la profession, à des vêtements ou à la position de travail (travail assis) peut avoir des conséquences sur la fertilité. La lumière, ou photopériode, a également une influence importante puisque des études ont montré que la production de spermatozoïdes était plus importante en hiver. Aux agents physiques s’ajoutent les facteurs psychosociaux comme le stress, le sport, le tabac, l’alcool, la nutrition et l’obésité qui ont un impact direct sur la fertilité (2 p.35). L’ensemble de ces facteurs, physiques, sociaux, alimentaires, métaboliques, ainsi que des prédispositions génétiques se combinent avec l’action propres des perturbateurs endocriniens dans des proportions qui restent à évaluer aujourd’hui.
La notion de Limite Maximale Résiduelle (LMR) est insuffisante…
La notion de LMR se construit à partir du produit, de sa toxicité individuelle, et de la Dose Journalière Admissible, à laquelle est supposé être exposé un individu sur la base d’un profil de consommation théorique. Mais l’ubiquité des perturbateurs endocriniens rend ce modèle inapplicable, et requiert un renversement de la stratégie d’enquête, sur le sujet lui-même, et la mesure de son exposition.“La notion d’exposition ne saurait être artificiellement scindée entre le milieu professionnel et d’autres milieux alors que la seule approche possible consiste à partir de l’individu exposé pour apprécier réellement l’impact sur sa santé des diverses expositions auxquelles il a été soumis au cours d’une journée, d’une année, de sa vie professionnelle ou de sa vie entière…La scission artificielle entre les expositions résultant de la vie professionnelle et celles dues à la vie privée recoupe en partie celle, tout aussi artificielle, opérée entre l’air extérieur et l’air intérieur. Aucune de ces deux scissions n’est pertinente (9 p.65).
…Pour rendre compte de la réalité des niveaux d’exposition
“Dans une étude de 2011 de l’Ineris et de l’I.N.V.S. visant à préparer la cohorte ELFE (étude longitudinale française depuis l’enfance) et qui va englober 20 000 nouveaux nés en 2011 jusqu’à leurs 18 ans, les chercheurs voulaient mesurer le taux d’imprégnation des mères par certains polluants. Or, ils ont mis en évidence des concentrations plus importantes en Bisphénol A et en phtalates pour les accouchements les plus médicalisés (césarienne, forceps) par rapport aux accouchements naturels par voie basse, moins médicalisés…Ces concentrations s’expliquent par les poches plastiques et les cathéters posés lors de ces accouchements et font apparaître l’exposition des femmes enceintes et des prématurés et nourrissons dans certaines circonstances du fait de leur hospitalisation” (2 p.80).La mesure de l’exposition des sujets à des substances présentes dans l’environnement sous de multiples aspects, corrélée avec la dangerosité du mécanisme d’action spécifique aux perturbateurs endocriniens, devrait suffire pour procéder à des évictions complètes de ces substances, et à leur remplacement par des substances ne présentant pas les mêmes dangers.
Effets transgénérationnels
“Dans un article publié en avril 2011, le Pr Charles Sultan et Nicolas Kalfa du CHRU Montpellier, ont montré que les petits-enfants, c’est-à-dire la 3e génération des femmes distilbène, ont 40 à 50 fois plus de chance de souffrir d’hypospadias. Soit une incidence de 0,2 % à 8,2 % pour les petitsenfants des « femmes Distilbène »” (2 p.81).Des phénomènes transgénérationels ont également été répertoriés chez les rongeurs pour d’autres substances. Une étude a montré l’impact négatif d’une exposition à la vinclozoline des femelles rongeurs gestantes sur le nombre de spermatozoïdes de leurs descendants mâles sur quatre générations (2 p.81). “ Une des spécificités de la lignée germinale est la transmission non seulement du génome mais également d’une mémoire épigénétique à la génération suivante. Il a été montré récemment qu’une exposition transitoire au cours de l’organogenèse gonadique à deux perturbateurs endocriniens, la vinclozoline ou le méthoxychlore, réduit la fertilité et la production de sperme du testicule adulte (Anway et coll., 2005). De manière frappante ce phénotype est transmis à travers la lignée germinale mâle sur au moins quatre générations sans exposition additionnelle. Ce phénotype a été associé à une modification globale de la méthylation du génome dans la lignée germinale mâle” (4 p.152).
Effets à l’échelle des populations
“Dans certains cas, des substances peuvent avoir des effets qui ne sont pas pathologiques à l’échelle individuelle mais sont délétères à l’échelle de la population. C’est en particulier le cas d’un effet sur le sexratio. À titre d’exemple, un effet possible sur le sexratio dans l’espèce humaine de polluants persistants, dont certains sont des perturbateurs endocriniens, tels que le plomb (Simonsen et coll., 2006) ou la dioxine (Mocarelli et coll., 2000) a été rapporté” (4 p.157).
En conclusion de ce chapitre, il apparaît que les perturbateurs endocriniens sont des substances dont les mécanismes d’action ont mis en difficulté les modèles interprétatifs de la toxicologie et de l’épidémiologie. Ils sont néanmoins suffisamment identifiés aujourd’hui pour que l’impact spécifique des perturbateurs endocriniens, parmi les multiples facteurs polluants de notre environnement moderne soit bien reconnu par la communauté scientifique, la Société Internationale d’Endocrinologie, l’OMS[14], le CIRC[15]. L’urgence est désormais du côté de l’action politique, en vue de supprimer les agents toxiques perturbateurs endocriniens de l’environnement. Mais le retard au diagnostic, lié à une difficulté épistémologique se double aujourd’hui d’un retard réglementaire. En effet, les juridictions s’appuient sur des représentations de la causalité traditionnelles, qui ne reconnaissent pas les limites du modèle classique pour rendre compte de la toxicité des perturbateurs endocriniens. Les institutions tardent à réglementer en s’appuyant sur « le manque de preuves ». La science est prise au piège de dispositifs de causalité obsolètes, appliqués de manière dogmatique par des les institutions, au péril des peuples.
Pour en savoir plus sur les moyens de vous protéger des perturbateurs endocriniens, consultez notre ouvrage: L’homme, une espèce et un genre à protéger.
Dr Claire Condemine-Piron Présentation de l’auteur
[1] Déclaration de Wingspread https://docplayer.fr/58201368-La-declaration-de-wingspread.html http://reseau-environnement-sante.fr/wp-content/uploads/2016/01/LA_DECLARATION_DE_WINGSPREAD.pdf
[2] Sénat, rapport sur les perturbateurs endocriniens, 2011:http://www.senat.fr/rap/r10-765/r10-7651.pdf p.34
[3] Cinétique : étude de la vitesse des réactions chimiques
[4] INSERM, rapport Reproduction et Environnement, 2011: http://www.ipubli.inserm.fr/bitstream/handle/10608/222/expcol_2011_reproduction_Vc.pdf?sequence=1447 préface
[5] Pour la science, n°396, octobre 2010, p.42 et s. 2 Bouskine, Env. Health Perspect, 2009. 3 Ralph et al. Envrion Health Perspect, 11 :461-466 (2003). P.12
[6] ANSES: avis relatif aux critètes de définition des perturbateurs endocriniens, 2016: https://www.anses.fr/fr/system/files/SUBCHIM2016SA0133.pdf p.59
[7] Slama R., Bourguignon J.P., Demeneix B.A., Panzica G., Kortenkamp A., Zoeller T. (2016) Scientific issues relevant to setting regulatory criteria to identify endocrine disrupting substances in the European Union. Environ Health Perspect; doi: 10.1289/EHP217.
[8] IGAS: rapport sur la stratégie nationale sur les perturbateurs endocriniens, 2017: http://www.igas.gouv.fr/IMG/pdf/2017-117R.pdf
[9] Rapport de Mme Marie-Christine BLANDIN, fait au nom de l’Office parlementaire d’évaluation des choix scientifiques et technologiques n° 176 tome I (2007-2008) – 23 janvier 2008 http://www.assemblee-nationale.fr/13/pdf/rap-off/i0629-tI.pdf
[10] Epigenetic Transgenerational Actions of Endocrine Disruptors by Dr. Michael K. Skinner & Matthew D. Anway Epigenetic Transgenerational Actions of Endocrine Disruptors Matthew D. Anway and Michael K. Skinner Center for Reproductive Biology, School of Molecular Biosciences, Washington State University, Pullman, Washington 99164
[11] Klip H, Verloop J, van Gool JD, Koster ME, Burger CW, van Leeuwen FE; OMEGAProject Group. Hypospadias in sons of women exposed to diethylstilbestrol inutero: a cohort study. Lancet. 2002 Mar 30;359(9312):1102-7. PubMed PMID:11943257.https://www.ncbi.nlm.nih.gov/pubmed/11943257
[12] Environmental Health perspectives, site internet https://ehp.niehs.nih.gov/doi/10.1289/ehp1314
[13] ANSES: avis relatif aux critètes de définition des perturbateurs endocriniens, 2016: https://www.anses.fr/fr/system/files/SUBCHIM2016SA0133.pdf p.4
[14] OMS : Organisation Mondiale de la Santé
[15] CIRC : Centre International de Recherche sur le Cancer